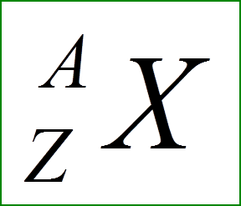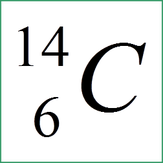Atomi i jezgro atoma
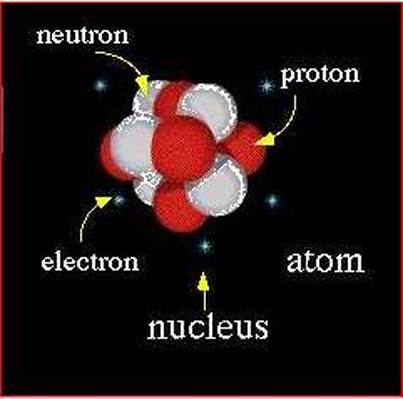
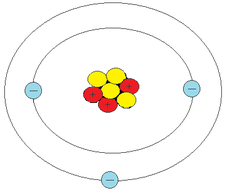
Atom se sastoji od jezgra (nukleusa) i elektronskog omotača, tj. od skupa elektrona raspoređenih oko jezgra.
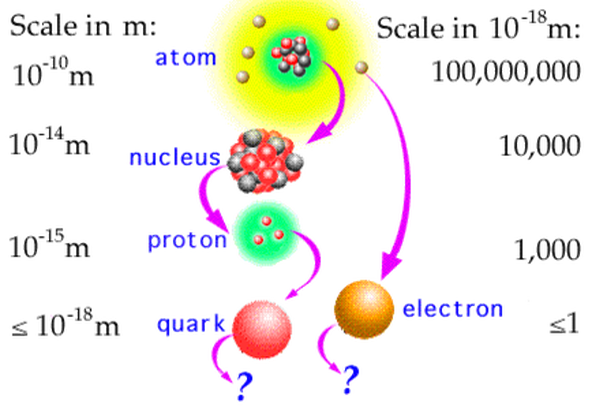
Atomsko jezgro se sastoji od dve vrste čestica- protona i neutrona, približno istih masa. Jedan proton ili jedan neutron ima oko 1840 puta veću masu od elektrona.
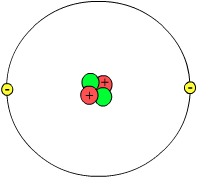
Protoni i elektroni su naelektrisani jednakim količinama elektriciteta suprotnog znaka.
Broj protona u atomu uvek je jednak broju elektrona, pa je svaki atom elektro-neutralan.
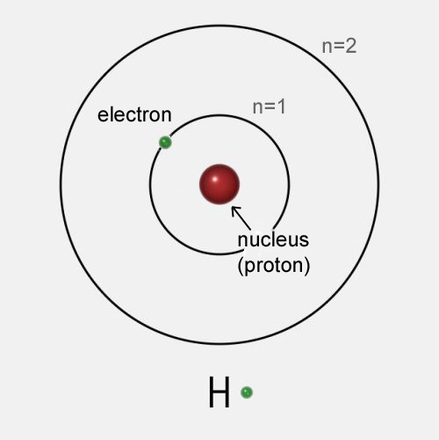
Model atoma naziva se planetarni model atoma. Najjednostavniji atom po strukturi je atom vodonika (1 proton u jezgru i 1 elektron u omotaču)
Broj protona ili elektrona u atomu predstavlja njegov redni broj u Periodnom sistemu elemenata (Z).
Ukupan broj protona i neutrona u jezgru (nukleona) čini maseni broj (A).
Ukupan broj protona i neutrona u jezgru (nukleona) čini maseni broj (A).
Oznaka atomskog jezgra je:
Primer:
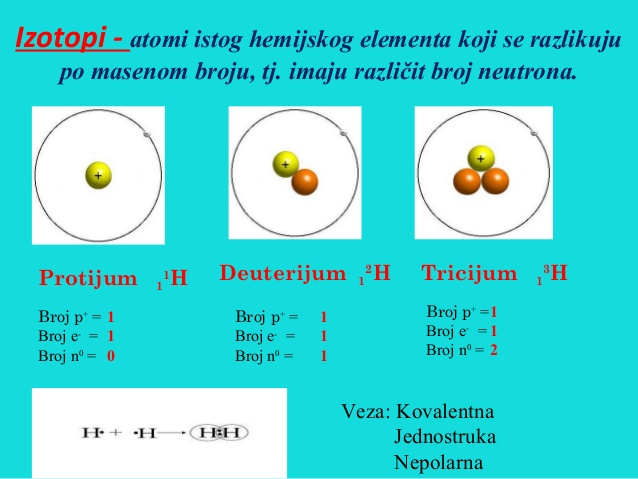
Neki elementi mogu imati u jezgru različiti broj neutrona, čime se ne menjaju njihove hemijske osobine, ali im se menja atomska masa i oni se nazivaju izotopi.
Primer:
Primer:
Ako se iz elektronskog omotača izdvoji elektron, on postaje slobodan elektron, a atom- pozitivan jon.
Ako atom zahvati jedan slobodan elektron onda on postaje negativan jon.
Ako atom zahvati jedan slobodan elektron onda on postaje negativan jon.
Između protona u jezgru vladaju odbojne električne sile. Međutim, jezgro se ne raspada jer između nukleona u jezgru deluju i nuklearne sile.
Nuklearna interakcija je privlačna i oko 100 puta jača od električne. Ona je kratkog dometa (deluje na blizinu). Nuklearna sila ne zavisi od vrste nukleona.
Nuklearna interakcija je privlačna i oko 100 puta jača od električne. Ona je kratkog dometa (deluje na blizinu). Nuklearna sila ne zavisi od vrste nukleona.